|
|
MALADIE DE PARKINSON IDIOPATHIQUE (M.P.I.)
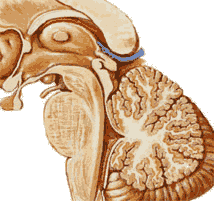
LA VOIE NIGRO-STRIATALELes neurones de la substance noire libère à destination du Striatum un messager chimique,La Dopamine, qui
L'atteinte de la boucle dopaminergique nigro-striatale est le principal mécanisme des syndromes extra-pyramidaux. Différentes structures participent au contrôle des mouvements: Striatum (noyau caudé - Putamen - Pallidum), thalamus, noyaux sous-thalamiques et noyaux rouges. Constitutifs du système extra-pyramidal, ils contribuent à la régulation du tonus, l'initiation des mouvements volontaires et l'adaptation posturale.
CRITERES CLINIQUESLes critères cliniques habituellement retenus sont :
SYMPTÔMES ASSOCIES à la MPI
EVOLUTIONOn décrit classiquement trois étapes évolutives de la M.P.I. :
TRAITEMENTS
Les choix thérapeutiques sont essentiellement guidés par :
MEDICAMENTSEn 1950 : découverte de la DopamineEn 1960 : mise en évidence du rôle de la Dopamine La MPI devient la première maladie attribuée à la déficience d'un neuro-transmetteur. En 1967 : (capable de traverser la barrière hémato-encéphalique) Son action est spectaculaire assortie toutefois d'effets secondaires invalidants : nausées, vomissements, irritabilité, hyperactivité, mouvements incontrôlables (dyskinésies Dopa-induites) et hallucinations THERAPIES CELLULAIRESLa greffe neuronale consiste à introduire dans le Striatum des cellules nerveuses embryonnaires capables de se différencier une fois en place en neurones aptes à synthétiser de la Dopamine.Une étude clinique est actuellement en cours. La greffe de cellules génétiquement modifiées. La thérapie génique consiste à introduire dans les neurones du striatum (à l'aide d'un vecteur - virus inactivé - ) un gène porteur d'un facteur neuro trophique. Les résultats sur le rat sont encourageants. TRAITEMENTS CHIRURGICAUX
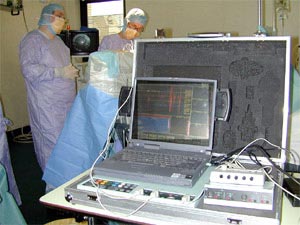
Stimulation thalamique chronique depuis 1987. L'action sur la cible thalamus n'est efficace que sur le tremblement et ne permet pas de réduire la L-dopa. Utilisée plus particulièrement sur les tremblements essentiels. La pallidotomie proposée par Leksell en 1956. Très en faveur aux USA. Efficace sur les dyskinésies dopa-induites. Risques d'effets secondaires non réversibles. LA STIMULATION DU NOYAU SOUS THALAMIQUECette technique a été mise au point par l'équipe du Pr. A. Louis BENABID de Grenoble en 1993.La destruction des neurones dopaminergiques de la SN rendent certaines zones du striatum hyper ou hypo-actives. Ainsi, le noyau sous thalamique (qui intervient dans la boucle de commande motrice) devient hyper actif. En le stimulant à l'aide de micro électrodes, son activité est bloquée, ce qui se traduit par une amélioration très nette de l'akinésie et de la rigidité. Efficace sur la triade parkinsonienne. Elle permet une forte diminution de la dopamine. CRITERES DE SELECTION
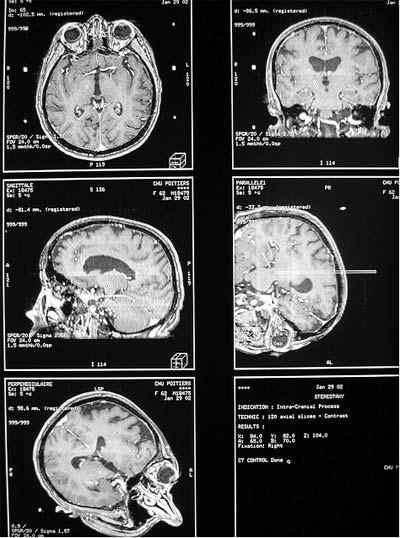
PLACE DE L'IMAGERIE
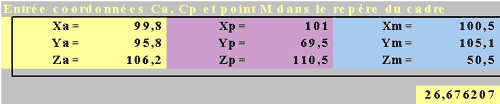
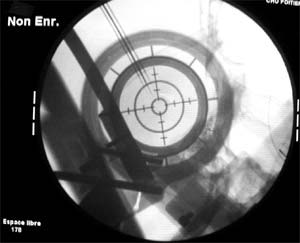
LES SEQUENCESCentrage sur le milieu du cadre.Repérage coro et sagittal
TRAITEMENTS DES IMAGESIl se fait sur une console GE. ADW 3.12 logiciels indispensables : REFORMAT et STEREOTAXY
TRAITEMENTS DES IMAGES
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
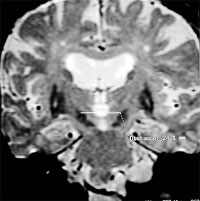
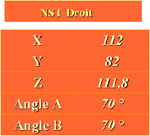
| CORO T2 : Mesures à effectuer Coordonnées NST droit et gauche Coordonnées Ca, Cp et M Distance inter NST |
|
|
|
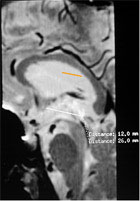
Distance Cp - inter NST
|
||
|
|
|
|
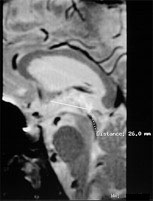
Distance Ca - Cp
|
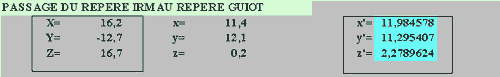

| Séquence 3D TOF gado Logiciel STEREOTAXY |
|
|
|
|

|
|
|
|
|
|
|
|
|
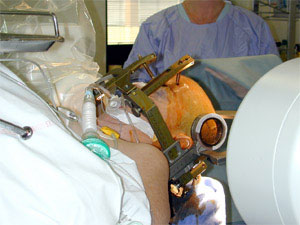
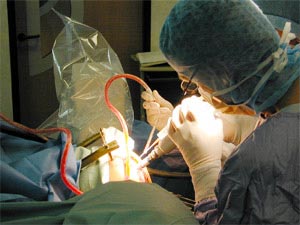
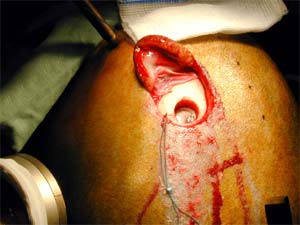
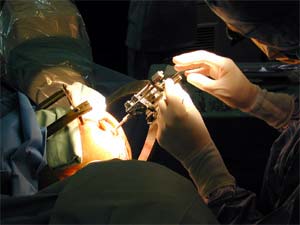
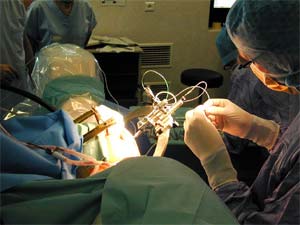
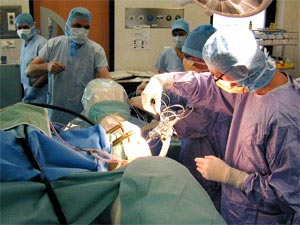
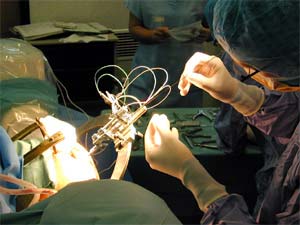
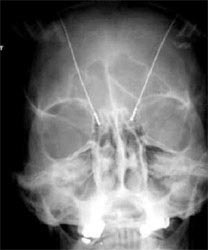
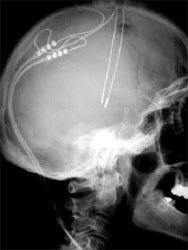
Électrode test

|
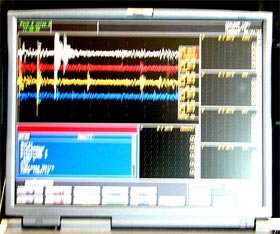
| L'activité des électrodes est enregistrée. La qualité de la réponse définira la position de l'électrode définitive. |
|
|
|